廣東病理切片
未來發展趨勢將聚焦的三大方向:①超多重染色(>30色)技術的標準化流程;②術中智能診斷系統(如5G遠程冰凍切片分析);③類***藥物敏感性測試的自動化染色平臺。隨著IVD認證的推進(如FDA已批準7款病理AI軟件),這些新技術有望在2030年前覆蓋80%的常規病理診斷場景下,推動病理學進入"精細智能診斷"新時代。實驗室需提前布局數字化基礎設施(如千兆級病理圖像存儲系統)和復合型人才培養,用來迎接技術變革帶來的機遇與挑戰。六胺銀染色能凸顯肺組織中的肺孢子菌,對免疫功能低下患者的機遇性**診斷至關重要。廣東病理切片

巴氏染色法(Papanicolaou staining)是細胞病理學中**重要的染色技術之一,尤其作為婦科宮頸脫落細胞學檢查的金標準。該染色方法通過多色染液的階梯式組合,能夠精細區分細胞的不同分化狀態和病理改變。染色過程嚴格分為五個階段:首先使用蘇木精染液(通常為Harris蘇木精)對細胞核進行5-10分鐘的染色,使核染色質呈現清晰的深藍色;接著用0.5%鹽酸酒精分化去除胞質多余染料,再通過稀碳酸鋰溶液返藍;然后依次浸入橘黃G6染液(2-3分鐘)和EA50染液(5分鐘),這兩種染液的特殊配方能使角化細胞呈現醒目的橙紅色,非角化細胞顯示藍綠色,而中間層細胞則呈現過渡性的藍紫色。貴州哪里有病理切片銷售電話熒光染料DAPI可特異性標記細胞核,在流式細胞術或細胞凋亡檢測中作為基礎染色方法。
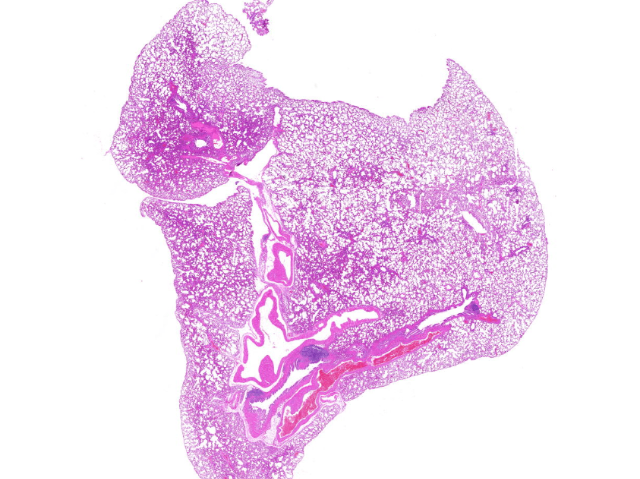
該染色法的診斷價值主要體現在對組織纖維化的評估上:在肝硬化標本中,可清晰顯示門靜脈區增生的藍色膠原纖維包繞紅色肝細胞團;在肺纖維化組織,能明確區分肺泡間隔內異常沉積的藍色膠原纖維與正常肺間質結構;在心肌梗死后修復過程中,可準確識別紅色存活心肌與藍色瘢痕組織的界限。此外,Masson染色還能幫助鑒別**間質反應程度,如浸潤性乳腺*中可見*細胞巢被藍色膠原纖維包繞,而平滑肌肉瘤則表現為彌漫的紅色肌源性分化區域。現代數字化病理分析系統常基于Masson染色結果進行膠原面積定量,為纖維化疾病的療效評估提供客觀指標。該技術因其穩定的染色效果和明確的組織對比度,至今仍是結締組織病理診斷的基石性方法。
近年來,隨著分子病理學和人工智能技術的深度融合,病理切片染色技術正經歷**性變革。多重免疫熒光染色(mIHC/mIF)通過光譜分離技術(如Opal 7色系統)可在單張切片上同步檢測PD-L1/CD8/FOXP3等7種標志物,結合多光譜成像系統(如Vectra Polaris)實現**微環境免疫細胞亞群的精確定量,其空間分辨率可達0.25μm/pixel,較傳統IHC診斷效率提升5倍以上。數字病理與AI分析已進入臨床實用階段,如谷歌DeepMind開發的乳腺*淋巴結轉移檢測系統(靈敏度達99.3%),可對全切片圖像(WSI)進行實時分析,自動標注可疑區域并生成結構化報告。納米金標記技術通過表面等離子共振增強信號,顯著提高原位雜交檢測的靈敏度和分辨率。
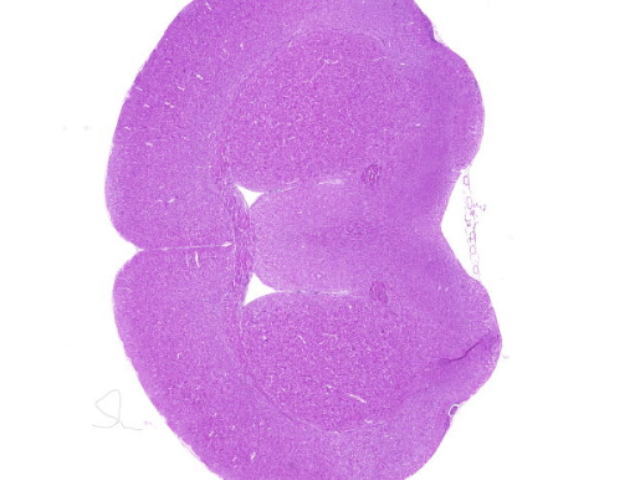
PAS染色中糖原檢測的假陰性問題主要源于三個關鍵環節的失控:氧化不充分、Schiff試劑失效和切片厚度不當。在氧化步驟中,必須使用新鮮配制的1%高碘酸溶液(避光保存≤2周),氧化時間嚴格控制在10-15分鐘(室溫20-25℃)。當檢測富含糖原的組織(如肝組織或橫紋肌)時,建議每5分鐘顯微鏡下觀察氧化程度,直至基底膜呈現輕微膨脹狀態(提示多糖充分暴露)。Schiff試劑的有效性可通過空白對照試驗驗證:滴加試劑于已知陽性組織,30分鐘內未出現紫紅色反應即提示失效(正常試劑應使糖原在5分鐘內顯色)。多重免疫熒光技術通過光譜分離實現多靶標檢測,顯著提高**微環境分析的效率和準確性。浙江肝臟病理切片
量子點標記技術利用納米顆粒提高信號強度,在低表達靶標的超敏檢測中展現明顯優勢。廣東病理切片
油紅O染色的**診斷價值體現在代謝性疾病的評估中:在非酒精性脂肪肝(NAFLD)標本中,可清晰顯示肝細胞胞質內大小不等的橙紅色脂滴,根據脂滴融合程度可區分單純性脂肪變(微泡型)與脂肪性肝炎(大泡型);在***斑塊中,能特異性標記泡沫細胞內的膽固醇酯沉積;在脂肪肉瘤診斷時,可鑒別高分化脂肪肉瘤(彌漫陽性)與其他梭形細胞**。該技術對肥胖相關研究尤為重要,通過圖像分析系統量化染色面積,可精確計算脂肪組織占比。操作中需特別注意:①染液需現配現用,久置易形成沉淀導致背景染色;②避免使用有機溶劑封片,推薦水性封片劑如甘油明膠;③陰性對照需同步進行異丙醇脫脂處理以驗證特異性。現代改良法可與免疫熒光聯用,實現脂肪沉積與炎癥標志物的共定位分析。廣東病理切片
- 甘肅哪里有科研一抗銷售方法 2025-11-06
- 中國澳門動物試驗ELISA試劑盒怎么樣 2025-11-06
- 山西進口ELISA試劑盒咨詢報價 2025-11-06
- 天津小鼠病理切片實驗效果 2025-11-06
- 寧夏附近哪里有ELISA試劑盒 2025-11-06
- 江蘇豬科研一抗電話多少 2025-11-06
- 湖北魚科研一抗型號 2025-11-06
- 河北ELISA試劑盒一般多少錢 2025-11-06
- 中國澳門PAS染色全景掃描 2025-11-06
- 北京犬ELISA試劑盒 2025-11-06
- 河南醫療產品體系建設 2025-11-06
- 北京點射光纖半導體激光治療儀1470nm波長光纖傳導直達病灶 2025-11-06
- 一次性醫療監測設備EO滅菌費用 2025-11-06
- 北京綜合高鹽核酸酶價格表 2025-11-06
- 海南UN38.3電池包 2025-11-06
- 兒童脊柱評估系統定制 2025-11-06
- 廣東指骨夾板大概多少錢 2025-11-06
- 天津本地醫用刻錄機技術指導 2025-11-06
- 浙江強腦智能假肢哪家便宜 2025-11-06
- 江蘇短鼻拭子廠商 2025-11-06