全人源單重鏈合成文庫篩選流程
全人源VHH合成文庫實現了免疫原性從“異源風險”到“全人源安全”的轉變。全人源VHH合成文庫的抗體序列完全源自人類IGHV基因家族,人源化率超過98%,從根源上規避了鼠源或嵌合抗體的免疫原性風險,臨床應用時無需額外進行人源化改造,可直接用于臨床前及臨床研究,尤其適合需要長期用藥的場景。而傳統平臺如鼠源scFv或轉基因小鼠抗體,因含有鼠源成分,易引發人體抗藥物抗體(ADA)反應,往往需通過CDR移植等復雜改造流程,不僅耗時6-12個月,且改造成功率不足50%。已有抗PD-L1VHH藥物憑借全人源特性順利進入臨床Ⅰ期,全程未檢測到ADA,而某鼠源scFv藥物卻因免疫反應被迫終止于臨床Ⅱ期。上海溪長生物技術全人源 VHH 合成文庫,更優的篩選流程提高開發效率。全人源單重鏈合成文庫篩選流程
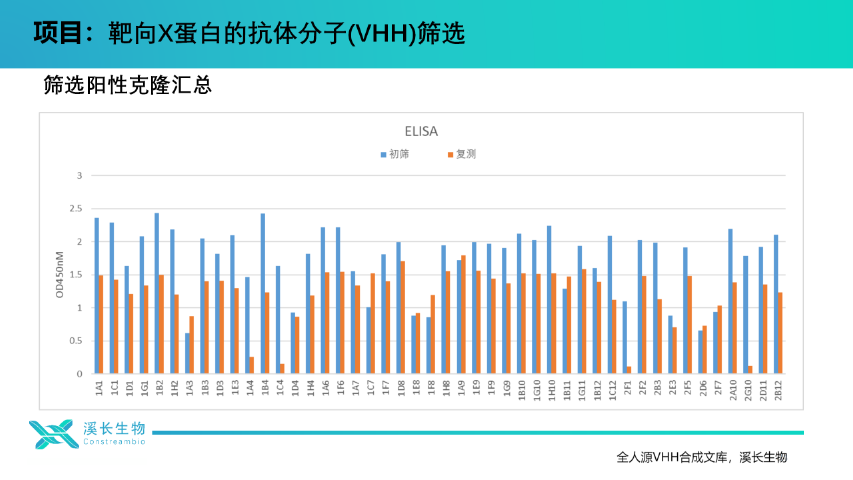
VHH作為駱駝科動物特有的單鏈抗體,具有分子量小(約15kDa)、組織穿透性強、穩定性高的特點,在病毒中和、成像診斷等領域表現出獨特潛力。全人源VHH合成文庫將逐步替代部分傳統單克隆抗體,尤其在實體瘤、神經疾病等領域憑借穿透性優勢占據主導。同時,其與基因治療、細胞治療的融合應用(如作為AAV靶向配體)將加速遺傳病和罕見病治療的突破。此外,合成文庫結合高通量篩選的模式,可明顯降低中小企業的創新門檻,推動生物制藥創新生態的民主化,使抗體研發從“少數企業”走向“更廣的科研普惠”。陜西全人源單重鏈合成文庫哪家強上海溪長全人源VHH合成庫,應用范圍廣,服務經驗豐富。
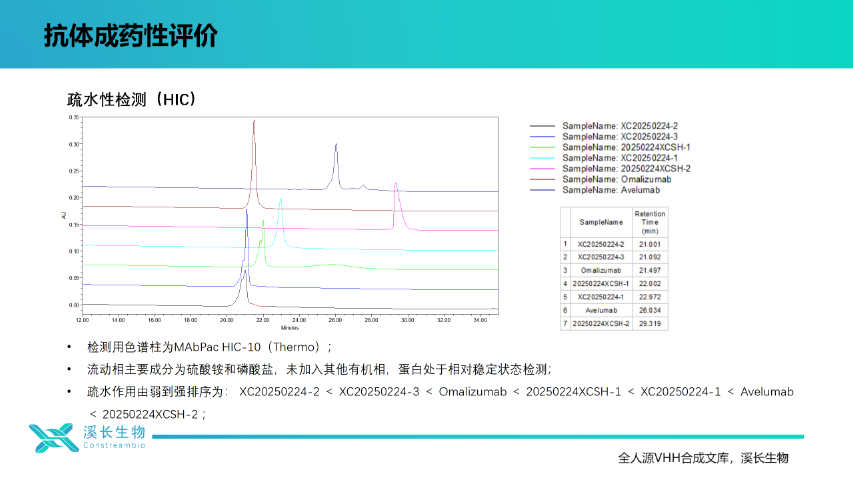
上海溪長生物全人源VHH合成文庫以其突出的性能,在抗體研發領域獨樹一幟。全人源的基因背景使得抗體在人體內的免疫原性極低,極大地提高了抗體藥物的安全性和有效性,為臨床治療帶來了更高的保障。文庫構建過程中運用了先進的隨機化技術,使CDR區域的多樣性得到了充分的挖掘,能夠產生針對各種抗原的高親和力抗體,無論是常見的疾病靶點還是罕見病的特殊靶點,都能準確應對。VHH抗體的小分子量特點使其具有出色的組織穿透性,不僅能夠高效穿透實體瘤組織,實現對腫瘤細胞的有效打擊,還能跨越血腦屏障,為神經系統疾病的治療提供了新的解決方案。
產學研深度融合,溪長生物打造抗體開發"中國方案",溪長生物聯合上海交大、復旦大學等科研機構,構建"基礎研究-技術開發-產業轉化"創新鏈條。全人源VHH合成文庫作為關鍵技術載體,合作開發不同靶點抗體分子。開展靶點驗證與抗體初篩;技術開發階段,雙方聯合優化篩選策略,達成合作共贏的一致共識。在篩選的同時提供抗體優化的專業指導,全程助力科研人員快速獲得高特異性、高親和力的VHH抗體,加速抗體藥物從實驗室走向臨床的步伐。上海溪長全人源 VHH 合成文庫,兼容多場景抗體開發。

在抗體研發領域,全人源單結構域VHH合成文庫正成為創新突破的關鍵利器。相較于傳統抗體文庫,全人源單結構域VHH合成文庫具備獨特優勢。其基于全人源序列設計,有效降低免疫原性風險,適配臨床治療性抗體開發需求。單結構域VHH分子量小、結構簡單,可穿透深層組織,結合特殊抗原表位,在自身免疫病等疾病靶點探索中,能挖掘常規抗體難以觸及的結合位點。文庫構建依托先進基因合成與篩選技術,涵蓋豐富序列多樣性,可快速篩選高親和力、高特異性VHH分子。無論是藥物研發企業加速抗體藥物管線推進,還是科研團隊開展前沿抗體機制研究,溪長生物的全人源單結構域VHH合成文庫助力突破研發瓶頸,開啟抗體設計與高效篩選的全新篇章,為生物醫藥創新發展注入強勁動力。上海溪長全人源 VHH 合成文庫,適配雙特異性 VHH 開發,一鍵串聯抗原結合域,多功能分子設計更靈活!全人源單重鏈合成文庫篩選流程
全人源 VHH 合成文庫,上海溪長技術加持,抗體發現效率翻倍。全人源單重鏈合成文庫篩選流程
駱駝科動物的血清同時含有常規的異四聚體抗體和獨特的功能性重(H)鏈抗體(HCAb)。這些同二聚體抗體的H鏈由一個抗原結合結構域,納米抗體(VHH)和兩個恒定結構域(CH2,CH3區)組成。由于恒定結構域的缺失和納米抗體(VHH)側的重塑表面(通常與常規抗體中的L鏈相關),HCAb不能摻入輕(L)鏈。已經鑒定了構成HCAb的遺傳元件,但是仍在很大程度上對將這些抗體從其基因體內生成為抗原特異性和親和力成熟的真正抗體進行研究。然而,由多個晶體結構支持的抗原特異性VHH的簡便鑒定及其有益的生化和經濟特性(大小,親和力,特異性,穩定性,生產成本)鼓勵了將這些單域抗體用作研究工具以及生物技術和醫學的抗體工程化。全人源單重鏈合成文庫篩選流程
- 江西全人源單結構域(VHH)合成文庫服務方案 2025-11-07
- 中國臺灣Fab合成文庫哪家強 2025-11-07
- 貴州VHH合成文庫應用 2025-11-06
- 中國臺灣合成文庫 2025-11-06
- 陜西噬菌體文庫成本 2025-11-06
- 安徽單結構域文庫服務方案 2025-11-06
- 西藏噬菌體文庫技術應用 2025-11-06
- 河南全人源單重鏈合成文庫技術應用 2025-11-06
- 黑龍江單結構域文庫篩選方案 2025-11-06
- 河北全人源單重鏈合成文庫篩選時間 2025-11-06
- 廣西滅菌咽拭子出口企業 2025-11-07
- 山西醫院菌群移植臨床應用 2025-11-07
- 胰酪胨大豆瓊脂培養基生產 2025-11-07
- 坪山區標準體外診斷試劑工廠直銷 2025-11-07
- 青浦區高韌性尼龍 2025-11-07
- 裂殖壺菌藻油DHA原料是什么 2025-11-07
- 廣西2.0mm厚度成型片定制廠家 2025-11-07
- 青海腹瀉使用菌群移植耗材 2025-11-07
- 鎮江綠地智能醫療穿戴設備收費 2025-11-07
- 實驗室蛋白質組學自動化設備 2025-11-07